GC녹십자, 간이식 대체 혁신 치료제 국내 개발·상용화… 美 미럼 ‘마라릭시뱃’ 라이선스 계약
동아닷컴 김민범 기자
입력 2021-07-27 13:17 수정 2021-07-27 13:27
‘마라릭시뱃’ 소아 희귀 간질환 치료제
2019년 美 FDA 혁신 치료제 지정
GC녹십자, 내년부터 국내 승인 절차 추진

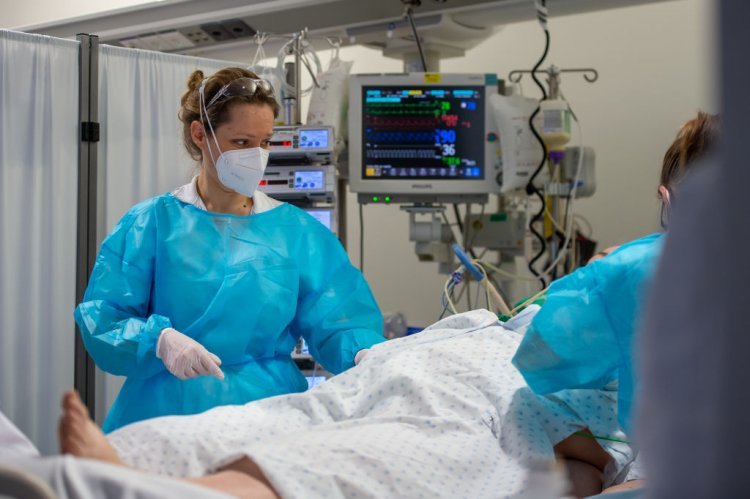
GC녹십자는 미국 미럼파마슈티컬스(Mirum Pharmaceuticals, 이하 미럼)와 소아 희귀간질환 신약인 ‘마라릭시뱃(Maralixibat)’ 개발 및 상용화를 위한 독점 라이선스 계약을 체결했다고 27일 밝혔다.
미럼은 현재 마라릭시뱃의 알라질증후군(ALGS, 간 담도가 감소하고 담즙이 정체되는 희귀 유전 질환), 진행성 가족성 간내 담즙 정체증(PFIC, 담즙 배출 관여 단백질 유전적 결함으로 발생하는 질환), 담도 폐쇄증(BA, 간 밖으로 연결된 담도관이 파괴되거나 형성에 이상이 생겨 일부 또는 전부가 폐쇄되는 상태) 등 적응증에 대한 미국 및 유럽 허가 절차와 임상을 진행 중이다. 특히 전 세계적으로 ALGS와 BA 적응증에 대해서는 현재 간이식 외에 허가된 치료제나 치료법이 없는 상황이다.
마라릭시뱃은 지난 2019년 미국 식품의약국(FDA)으로부터 1세 이상 ALGS 환자의 소양증(pruritus)에 대한 ‘혁신 치료제(Breakthrough Therapy)’로 지정받았다. 올해 1월 품목 허가를 신청한 상태다. PFIC 타입2(type2) 적응증에 대해서도 유럽에서 품목 허가 절차가 진행되고 있다. BA 적응증에 대해서는 현재 글로벌 임상 2상이 진행 중이다.
이번 계약에 따라 GC녹십자는 마라릭시뱃에 대한 국내 독점 개발 및 상용화 권리를 확보하게 됐다. 내년 ALGS를 시작으로 순차적으로 3가지 적응증에 대한 국내 승인 절차에 돌입한다는 계획이다.
크리스 피츠(Chris Peetz) 미럼파마슈티컬스 대표는 “GC녹십자와 혁신 치료제 제공을 위한 비전을 공유하기로 했다”며 “희귀질환 치료제 상용화 경험이 있는 GC녹십자와 협업을 통해 한국에 치료제를 신속히 공급할 수 있게 되길 기대한다”고 전했다.
허은철 GC녹십자 대표는 “이번 협력은 소아 희귀질환 극복을 위한 중요한 이정표가 될 것”이라며 “국내 희귀질환 환자 삶의 질 향상을 위해 치료제의 조속한 상용화에 최선을 다하겠다”고 말했다.
동아닷컴 김민범 기자 mbkim@donga.com
2019년 美 FDA 혁신 치료제 지정
GC녹십자, 내년부터 국내 승인 절차 추진

GC녹십자는 미국 미럼파마슈티컬스(Mirum Pharmaceuticals, 이하 미럼)와 소아 희귀간질환 신약인 ‘마라릭시뱃(Maralixibat)’ 개발 및 상용화를 위한 독점 라이선스 계약을 체결했다고 27일 밝혔다.
미럼은 현재 마라릭시뱃의 알라질증후군(ALGS, 간 담도가 감소하고 담즙이 정체되는 희귀 유전 질환), 진행성 가족성 간내 담즙 정체증(PFIC, 담즙 배출 관여 단백질 유전적 결함으로 발생하는 질환), 담도 폐쇄증(BA, 간 밖으로 연결된 담도관이 파괴되거나 형성에 이상이 생겨 일부 또는 전부가 폐쇄되는 상태) 등 적응증에 대한 미국 및 유럽 허가 절차와 임상을 진행 중이다. 특히 전 세계적으로 ALGS와 BA 적응증에 대해서는 현재 간이식 외에 허가된 치료제나 치료법이 없는 상황이다.
마라릭시뱃은 지난 2019년 미국 식품의약국(FDA)으로부터 1세 이상 ALGS 환자의 소양증(pruritus)에 대한 ‘혁신 치료제(Breakthrough Therapy)’로 지정받았다. 올해 1월 품목 허가를 신청한 상태다. PFIC 타입2(type2) 적응증에 대해서도 유럽에서 품목 허가 절차가 진행되고 있다. BA 적응증에 대해서는 현재 글로벌 임상 2상이 진행 중이다.
이번 계약에 따라 GC녹십자는 마라릭시뱃에 대한 국내 독점 개발 및 상용화 권리를 확보하게 됐다. 내년 ALGS를 시작으로 순차적으로 3가지 적응증에 대한 국내 승인 절차에 돌입한다는 계획이다.
크리스 피츠(Chris Peetz) 미럼파마슈티컬스 대표는 “GC녹십자와 혁신 치료제 제공을 위한 비전을 공유하기로 했다”며 “희귀질환 치료제 상용화 경험이 있는 GC녹십자와 협업을 통해 한국에 치료제를 신속히 공급할 수 있게 되길 기대한다”고 전했다.
허은철 GC녹십자 대표는 “이번 협력은 소아 희귀질환 극복을 위한 중요한 이정표가 될 것”이라며 “국내 희귀질환 환자 삶의 질 향상을 위해 치료제의 조속한 상용화에 최선을 다하겠다”고 말했다.
동아닷컴 김민범 기자 mbkim@donga.com
비즈N 탑기사
 ‘투머치 토커’의 모자…민희진 폭주에 박찬호 소환 왜
‘투머치 토커’의 모자…민희진 폭주에 박찬호 소환 왜 백일 아기 비행기 좌석 테이블에 재워…“꿀팁” vs “위험”
백일 아기 비행기 좌석 테이블에 재워…“꿀팁” vs “위험” 최저임금 2만원 넘자 나타난 현상…‘원격 알바’ 등장
최저임금 2만원 넘자 나타난 현상…‘원격 알바’ 등장 “배우자에게 돈 보냈어요” 중고거래로 명품백 먹튀한 40대 벌금형
“배우자에게 돈 보냈어요” 중고거래로 명품백 먹튀한 40대 벌금형 이렇게 63억 건물주 됐나…김지원, 명품 아닌 ‘꾀죄죄한’ 에코백 들어
이렇게 63억 건물주 됐나…김지원, 명품 아닌 ‘꾀죄죄한’ 에코백 들어- 상하이 100년간 3m 침식, 中도시 절반이 가라앉고 있다
- 김지훈, 할리우드 진출한다…아마존 ‘버터플라이’ 주연 합류
- “도박자금 마련하려고”…시험장 화장실서 답안 건넨 전직 토익 강사
- 몸 속에 거즈 5개월 방치…괄약근 수술 의사 입건
- 일본 여행시 섭취 주의…이 제품 먹고 26명 입원
 한국에 8800억 투자 獨머크 “시장 주도 기업들 많아 매력적”
한국에 8800억 투자 獨머크 “시장 주도 기업들 많아 매력적” 직장인 1000만명 이달 월급 확 준다…건보료 ‘20만원 폭탄’
직장인 1000만명 이달 월급 확 준다…건보료 ‘20만원 폭탄’ 1인 가구 공공임대 ‘면적 축소’ 논란…국토부 “면적 기준 폐지 등 전면 재검토”
1인 가구 공공임대 ‘면적 축소’ 논란…국토부 “면적 기준 폐지 등 전면 재검토” “만원으로 밥 먹기 어렵다”…평균 점심값 1만원 첫 돌파
“만원으로 밥 먹기 어렵다”…평균 점심값 1만원 첫 돌파 고금리-경기침체에… 개인회생 두달새 2만2167건 역대 최다
고금리-경기침체에… 개인회생 두달새 2만2167건 역대 최다- 美-중동 석유공룡도 뛰어든 플라스틱… 역대급 공급과잉 우려[딥다이브]
- 카드사 고위험업무 5년 초과 근무 못한다…여전업권 ‘내부통제 모범규준’ 시행
- 작년 서울 주택 인허가, 목표치 33% 그쳐… 2, 3년뒤 공급난 우려
- 은행연체율 4년9개월만에 최고… 새마을금고 ‘비상등’
- 작년 4대그룹 영업이익 24.5조, 66% 감소…현대차그룹만 늘어












![美-중동 석유공룡도 뛰어든 플라스틱… 역대급 공급과잉 우려[딥다이브] 美-중동 석유공룡도 뛰어든 플라스틱… 역대급 공급과잉 우려[딥다이브]](https://dimg.donga.com/a/102/54/90/1/wps/ECONOMY/FEED/BIZN/124642003.3.thumb.jpg)





![우리 집앞에도 ‘연트럴파크’ 생길까?…철도 지하화 사업의 모든 것[부동산 빨간펜] 우리 집앞에도 ‘연트럴파크’ 생길까?…철도 지하화 사업의 모든 것[부동산 빨간펜]](https://dimg.donga.com/a/102/54/90/1/wps/ECONOMY/FEED/BIZN_REALESTATE/124653245.2.thumb.png)