셀트리온, ‘비후성심근증 신약’ 日업체와 판권 계약…美희귀의약품 지정 추진
동아닷컴 김민범 기자
입력 2019-03-25 10:24 수정 2019-03-25 10:27

셀트리온은 25일 비후성심근증(HCM, Hypertrophic Cardiomyopathy) 치료를 위해 개발 중인 신약 ‘CT-G20’에 대한 일본 독점 판권 계약을 현지 제약 업체와 체결했다고 밝혔다. 비후성심근증은 다른 증세 없이 좌심실 벽이 두꺼워지는 심장 질환으로 인구 500명당 1명 비율로 발견되는 것으로 알려졌다. 이번에 계약을 체결한 일본 업체는 내부 합의에 따라 일정 기간 공개하지 않기로 했다.
총 계약금액은 2500만 달러(약 283억 원) 규모로 계약 시점에 10%인 250만 달러(약 28억 원)를 셀트리온이 받게 된다. 상업화 과정에 따른 마일스톤 규모는 2250만 달러(약 255억 원)다. 신약 개발 과정에서 임상 및 허가 등 두 업체가 협의한 조건을 달성할 때마다 계약된 마일스톤을 수령한다.
이번 계약은 일반적인 제약업체 기술 수출과 다른 사업 모델로 신약 개발에 매진하면서 제품 소유권을 강화하고 유지하기 위한 조치라고 셀트리온 측은 강조했다. 국내를 비롯해 미국과 유럽 등 주요 시장에서는 셀트리온이 직접 제품을 판매할 계획이며 일본 등 다른 국가에서는 판권 계약 방식으로 사업을 추진한다는 방침이다.
셀트리온은 CT-G20 조기 글로벌 상업화를 위해 지난해 미국 FDA(식품의약국)와 품질과 비임상, 임상 등과 관련된 개발 전략에 대해 논의하는 미팅을 가졌다. 미팅을 통해 임상 개발 콘센트 논의가 완료된 상황이다. 현재 신약 개발 디자인 협의를 위한 2차 미팅을 준비 중이라고 회사 측은 설명했다.
국내에서는 다음 달 초 임상시험이 시작된다. 건강한 피험자를 대상으로 임상시험을 개시하고 올해 3분기에는 환자 대상 임상시험을 진행해 오는 2022년 말까지 3상을 종료한다는 계획이다. 생산은 셀트리온그룹 내 합성의약품 주요 생산기지를 갖춘 셀트리온제약이 맡는다. 글로벌 시장 제품 출시 목표 시기는 2023년으로 설정했다.
셀트리온 관계자는 “비후성심근증 치료제는 아직 글로벌 시장에 없는 신약으로 임상 비용 절감과 신속 심사가 가능한 미국 시장에서 신약 및 희귀의약품 지정 가능성을 타진할 계획”이라며 “CT-G20이 미국에서 신약 및 희귀의약품으로 지정받으면 7년간 시장 독점권을 갖게 된다”고 말했다.
한편 CT-G20 적응증인 비후성심근증은 좌측 심실 벽이 두꺼워지는 심장 질환이다. 비후성심근증 환자들은 좌심실 내강이 협소해지고 유출로가 폐색되면서 심장 이완 기능 저하와 심정지돌연사, 심부전 등 다양한 합병증을 얻기도 한다. 현재 글로벌 시장에서 비후성심근증 치료제로 공식 승인 받은 의약품은 없는 상황이다. 환자들은 호흡곤란과 피로감, 두근거림 등 증상 완화를 위해 고혈압약으로 사용되는 ‘베타차단제(beta blocker)’나 항부정맥 치료제를 처방 받고 있다.
주요 시장인 미국 내 비후성심근증 환자는 약 65만 명으로 추산된다. 1차 환자군인 폐쇄성 비후성심근증 환자는 약 60%로 40만 명에 달한다. 연간 인당 약제비는 약 2500만 원 수준으로 미국 내 치료제 시장 규모는 약 3조 원으로 보고 있다고 셀트리온 측은 전했다.
동아닷컴 김민범 기자 mbkim@donga.com
비즈N 탑기사
 “내가 먹은 멸치가 미끼용?” 비식용 28톤 식용으로 속여 판 업자
“내가 먹은 멸치가 미끼용?” 비식용 28톤 식용으로 속여 판 업자 ‘조폭도 가담’ 889억대 불법도박사이트 운영 일당 일망타진
‘조폭도 가담’ 889억대 불법도박사이트 운영 일당 일망타진 비오는 날 맨발로 옷가게 찾은 노숙자…새 신발 신겨 보냈더니
비오는 날 맨발로 옷가게 찾은 노숙자…새 신발 신겨 보냈더니 김숙 “내 건물서 거주+월세 수입 생활이 로망”
김숙 “내 건물서 거주+월세 수입 생활이 로망” “20억 받으면서 봉사라고?”…홍명보 감독 발언에 누리꾼 ‘부글’
“20억 받으면서 봉사라고?”…홍명보 감독 발언에 누리꾼 ‘부글’- 세계적 유명 모델이 왜 삼성역·편의점에…“사랑해요 서울” 인증샷
- “사람 치아 나왔다” 5000원짜리 고기 월병 먹던 中여성 ‘경악’
- “모자로 안가려지네”…박보영, 청순한 미모로 힐링 여행
- 엄마 편의점 간 사이 ‘탕’…차에 둔 권총 만진 8살 사망
- 8시간 후 자수한 음주 뺑소니 가해자…한문철 “괘씸죄 적용해야”
 “월세시대 열차 출발했다”…대출 규제 ‘풍선효과’
“월세시대 열차 출발했다”…대출 규제 ‘풍선효과’ 산청군, 여름휴가 여행지 만족도 전국 ‘2위’
산청군, 여름휴가 여행지 만족도 전국 ‘2위’ 오메가-3·오메가-6, 총 19가지 암 위험 감소 확인
오메가-3·오메가-6, 총 19가지 암 위험 감소 확인 농협-대상, 배추 상생마케팅 할인행사 실시
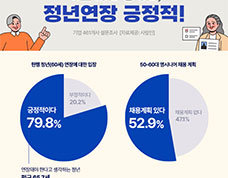
농협-대상, 배추 상생마케팅 할인행사 실시 기업 10곳 중 8곳 “정년 연장 긍정적”…평균 65.7세
기업 10곳 중 8곳 “정년 연장 긍정적”…평균 65.7세- 찬바람에 면역력 뚝… 예방접종으로 중증질환 대비를
- “종신보험 5∼7년 들면 최대 120% 환급”… 보험사 과열경쟁 논란
- 예비부부 멍드는 ‘묻지마 스드메’ 없앤다…내년부터 가격공개
- “급여의 25% 넘게 신용카드 썼다면, 남은 기간 체크카드 사용을”
- 서울 알짜 사업장에만 PF자금 몰려… 지방은 아직도 ‘부실 늪’