셀트리온, ‘램시마SC’ 54주 임상 결과 공개…“유효성·안전성 입증”
동아닷컴 김민범 기자
입력 2019-05-23 17:40 수정 2019-05-23 17:43
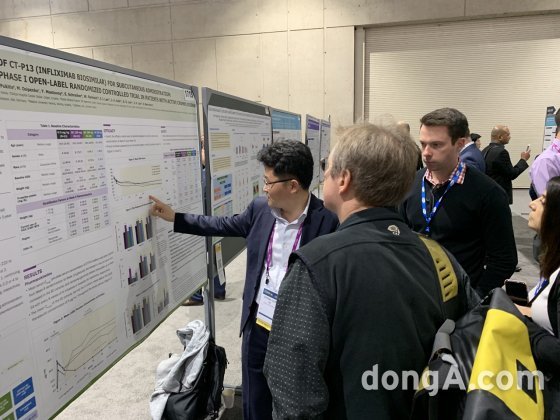
셀트리온에 따르면 연구진은 크론병 환자를 대상으로 인플릭시맙 바이오시밀러 램시마SC 제형의 적정 투여량을 확인했다. 54주 동안 램시마Ⅳ 제형과 안전성 및 유효성을 비교한 결과 램시마SC를 투여한 군의 체내 약물 농도가 램시마Ⅳ를 투여한 군에 비해 안정적으로 유지됐고 충분한 유효성을 보였다고 전했다. 또한 두 군의 안전성 평가 결과 데이터도 동등한 수준으로 나타난 것을 확인했다.
학회 포스터 세션에서 발표자로 나선 예병덕 서울아산병원 소화기내과 교수는 “인플릭시맙은 특히 염증성장질환(IBD) 분야에서 의료진과 환자 선호도가 높았지만 정맥주사 제형으로만 출시돼 편의성을 높인 피하주사 제형 개발을 기다려왔다”며 “램시마SC가 염증성장질환 치료제 시장에서 새로운 치료 대안이 될 것으로 예상된다”고 말했다.
램시마는 듀얼 포뮬레이션(Dual Formulation) 제형으로 개발돼 자가면역질환 환자에게 내원 초기에 정맥주사 제형으로 치료 효과를 극대화한다. 이후 피하주사 제형을 투여해 약효를 유지할 수 있어 편의성이 개선됐다. 피하주사 제형만을 투여 받는 환자는 초기 치료 시 적정 체내 약물 농도에 도달하기 위해 주사를 여러 차례 투여 받아야 한다.
셀트리온은 다양한 TNF-α억제제 제품군 내 정맥주사(Ⅳ) 제형과 피하주사(SC) 제형을 모두 갖춘 듀얼 포뮬레이션 제품 램시마의 편의성 및 염증성 장질환(IBD) 분야 강점을 활용한다는 방침이다. 이를 통해 한해 약 23조 원에 달하는 매출을 기록하고 있는 제품 ‘휴미라’ 등 경쟁제품의 염증성 장질환(IBD) 환자를 적극 유인한다는 전략이다.
셀트리온 관계자는 “학회 참석자들이 램시마SC 임상 과정 및 결과 발표를 통해 듀얼 포뮬레이션이라는 TNF-α억제제 분야의 새로운 치료 대안에 큰 기대감을 표시했다”며 “연내 램시마SC의 유럽의약품청(EMA, European Medicines Agency) 승인이 기대됨에 따라 시장에 빠르게 진입할 수 있도록 사전 출시 준비에 매진할 것”이라고 말했다. 이어 “미국에서도 조기 임상 완료와 허가를 위해 전력을 다하겠다”고 덧붙였다.
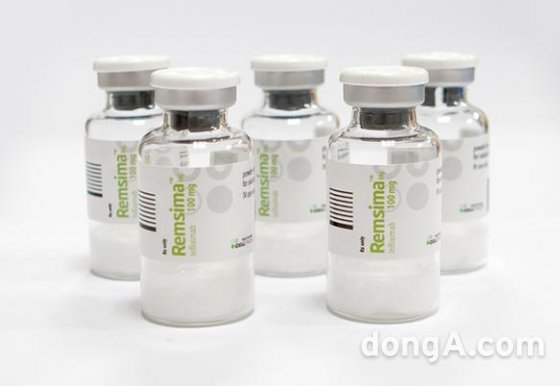
향후 램시마SC가 출시되면 이 같은 제형 시너지를 통해 인플릭시맙 글로벌 매출의 60%를 차지하고 있는 IBD 적응증 분야에서 더욱 강력한 시장 장악력을 확보할 수 있을 것으로 기대하고 있다. 특히 글로벌 43조 원 규모로 추산되는 TNF-α억제제 시장에서 전략적 우위를 점할 수 있을 전망이다.
한편 셀트리온은 오는 6월 스페인 마드리드에서 개최되는 유럽 최대 류마티스학회인 EULAR(The European League Against Rheumatism) 2019 학회에서 4년 동안 이뤄진 램시마Ⅳ 장기 안전성 입증 임상 결과와 램시마SC 제형 및 Ⅳ 제형 간 유효성, 약동학, 약력학 및 안전성 평가 결과를 담은 첫 임상 3상 결과를 발표할 예정이다.
셀트리온 측은 “유럽 램시마SC 허가가 순항 중이고 연내 허가 시점이 다가오고 있는 만큼 유럽 류마티스학회에서 램시마SC 임상 3상 결과 발표에 대한 의료 관계자들의 관심이 높아지고 있다”며 “학회 참석 및 발표를 계기로 유럽 시장에 램시마를 통한 새로운 치료 옵션 인지도를 높여갈 것”이라고 말했다.
동아닷컴 김민범 기자 mbkim@donga.com
















![[시승기] 제주에서 느끼는 드라이빙의 즐거움…‘포르쉐 올레 드라이브’ [시승기] 제주에서 느끼는 드라이빙의 즐거움…‘포르쉐 올레 드라이브’](https://dimg.donga.com/wps/ECONOMY/FEED/BIZN_FEED_EVLOUNGE/132703912.2.thumb.jpg)