종근당, 2세대 빈혈치료제 ‘CKD-11101’ 일본 판매 승인 신청
동아닷컴 김민범 기자
입력 2018-10-05 10:53 수정 2018-10-05 10:59
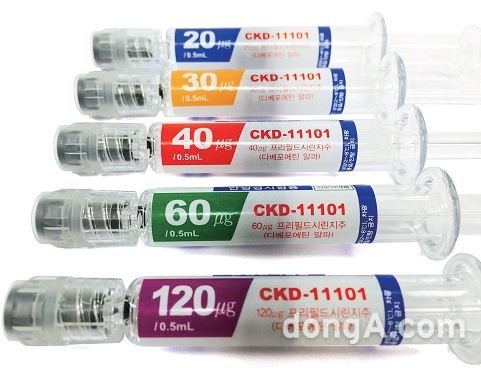
종근당은 2세대 빈혈치료제 바이오시밀러(유사 복제약) ‘CKD-11101’의 일본 내 제조판매를 위한 승인 신청을 후생노동성에 접수했다고 5일 밝혔다. CKD-11101은 지난 1일부터 일본에 수출이 시작됐다.
앞서 종근당은 미국 브랜드 제약회사 일본법인과 치료제 유통 허가를 위한 임상시험 진행과 제품허가, 제품 독점 판매 등에 대한 계약을 체결한 바 있다. 후생노동성으로부터 제조판매 승인을 받게 되면 종근당은 치료제 완제품을 미국회사 일본법인에 수출하고 이 법인은 현지 판매를 담당하게 된다. 미국회사 이름은 계약 상 노출할 수 없다고 종근당 관계자는 전했다.
CKD-11101은 다베포에틴 알파(Darbepoetin α)를 주성분으로 하는 네스프(원조 빈혈치료제) 바이오시밀러로 만성신부전 환자 빈혈치료에 효과적인 약물이다. 지난해 국내에서 임상시험을 마치고 식품의약안전처에 품목 허가를 신청했으며 올해 승인을 목표로 하고 있다. 식약처 승인이 완료되면 이 치료제는 종근당의 첫 번째 바이오의약품이면서 세계 최초의 네스프 바이오시밀러로 출시될 전망이다.
종근당 관계자는 “약 5000억 원 규모를 형성하고 있는 일본 네스프 시장에서 CKD-11101이 성공적으로 출시되고 시장을 확대할 수 있도록 미국 브랜드 일본법인과 협력을 강화할 것”이라며 “일본 시장을 바탕으로 향후 3조 원 규모 글로벌 네스프·아라네스프 시장에도 진출할 수 있을 것으로 기대한다”고 말했다.
한편 종근당은 CKD-11101 외에 지속형 단백질과 항체의약품 바이오시밀러와 바이오신약을 개발 중이다. 4조 원대 글로벌 시장을 형성하고 있는 황반변성 항체의약품 루센티스 바이오시밀러 ‘CKD-701’이 최근 식챡처로부터 임상 3상을 승인받아 서울대병원과 서울아산병원, 삼성서울병원 등 국내 25개 기관에서 임상시험을 진행할 예정이다. 항암이중항체 바이오신약 ‘CKD-702’는 범부처신약개발사업단 지원과제로 선정돼 전 임상 단계에 있다. 개발이 성공할 경우 기존 표적항암제 내성과 단점을 극복할 수 있는 혁신 신약이 될 것으로 예상된다.
동아닷컴 김민범 기자 mbkim@donga.com
















![[시승기] 제주에서 느끼는 드라이빙의 즐거움…‘포르쉐 올레 드라이브’ [시승기] 제주에서 느끼는 드라이빙의 즐거움…‘포르쉐 올레 드라이브’](https://dimg.donga.com/wps/ECONOMY/FEED/BIZN_FEED_EVLOUNGE/132703912.2.thumb.jpg)