김강립 “SK바사 백신, 임상2상 초기 데이터서 100% 중화항체”
뉴스1
입력 2021-10-08 15:44 수정 2021-10-08 15:45
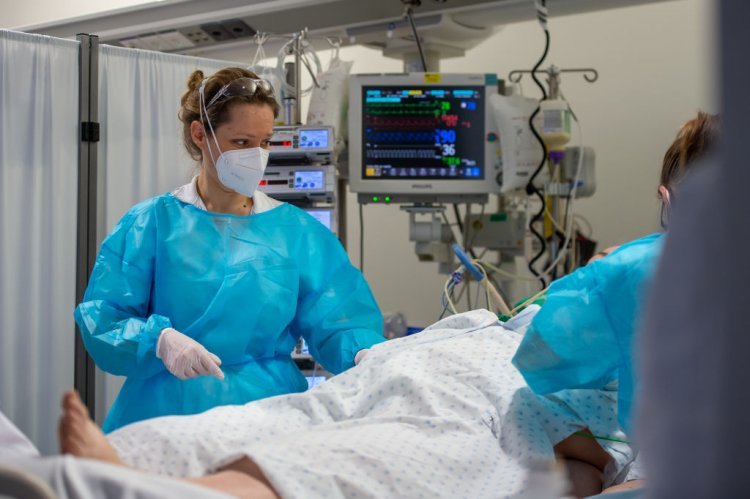
 김강립 식품의약품안전처 처장이 8일 서울 여의도 국회에서 열린 국회 보건복지위원회 국정감사에서 의원들의 질의에 답변하고 있다. 이날 김 처장은 앞으로 신종 코로나바이러스 감염증(코로나19) 예방백신, 치료제, 백신 주사기, 진단키트 등의 제품화 지원과 관리에 만전을 기하겠다는 입장을 밝혔다. (식약처 제공) 2021.10.8/뉴스1
김강립 식품의약품안전처 처장이 8일 서울 여의도 국회에서 열린 국회 보건복지위원회 국정감사에서 의원들의 질의에 답변하고 있다. 이날 김 처장은 앞으로 신종 코로나바이러스 감염증(코로나19) 예방백신, 치료제, 백신 주사기, 진단키트 등의 제품화 지원과 관리에 만전을 기하겠다는 입장을 밝혔다. (식약처 제공) 2021.10.8/뉴스1SK바이오사이언스가 개발 중인 코로나19 백신 ‘GBP510’이 임상2상 초기 단계에서 바이러스를 무력화하는 중화항체 100%를 형성하는 것으로 나타났다.
8일 열린 국회 보건복지위원회 국정감사에서 SK가 개발 중인 코로나19 백신이 아직 임상2상이 완료되지 않았음에도 3상을 승인한 게 특혜 아니냐는 질타와 관련해, 김강립 식약처장이 임상3상을 승인한 근거가됐다며 제시한 데이터다.
김강립 식약처장은 8일 열린 국정감사에서 “임상2상 전체 결과가 보고되진 않았지만, 2상에 대한 안전성 지표를 확인했고 피험자 100%에게 중화항체 (형성이) 확인됐다”고 말했다.
김 처장은 이어 “(중화항체 유도 수준은) 표준 혈청가의 5배 이상인 것으로 확인했기 때문에 나름의 근거, 과학적 판단으로 임상3상을 승인했던 것”이라고 덧붙였다.
이는 앞서 공개된 GBP510의 임상 1·2상 stage1 결과다. SK바이오사이언스는 10월 이후 임상2상 중간결과를 발표할 예정이다.
이날 이종성 국회 보건복지위원회 위원(국민의힘 의원)은 국감에서 “SK바이오사이언스는 임상2상이 끝나지도 않았는데, 지난 8월 3상 승인을 받았다”며 “의약품 안전성 확보보다 문재인 정부 성과물을 만들기 위해 무리한 것 아닌가”라고 질타했다.
이 위원은 이어 “이러한 백신, 치료제 허가과정에 특혜가 있는지 감사를 진행해도 되겠나”라고 덧붙였다.
김강립 처장은 “어떠한 의도를 갖고 서두르는 것은 전혀 없다”며 “모든 신약개발에 대해 같은 서비스를 제공하는게 맞지만, 코로나19라는 상황 아래, 국산 백신 개발이 식약처가 우선 집중, 지원해야 한다는 당위성이 충분히 근거가 된다고 판단한다”고 강조했다.
(서울=뉴스1)
비즈N 탑기사
 백일 아기 비행기 좌석 테이블에 재워…“꿀팁” vs “위험”
백일 아기 비행기 좌석 테이블에 재워…“꿀팁” vs “위험” 최저임금 2만원 넘자 나타난 현상…‘원격 알바’ 등장
최저임금 2만원 넘자 나타난 현상…‘원격 알바’ 등장 “배우자에게 돈 보냈어요” 중고거래로 명품백 먹튀한 40대 벌금형
“배우자에게 돈 보냈어요” 중고거래로 명품백 먹튀한 40대 벌금형 이렇게 63억 건물주 됐나…김지원, 명품 아닌 ‘꾀죄죄한’ 에코백 들어
이렇게 63억 건물주 됐나…김지원, 명품 아닌 ‘꾀죄죄한’ 에코백 들어 상하이 100년간 3m 침식, 中도시 절반이 가라앉고 있다
상하이 100년간 3m 침식, 中도시 절반이 가라앉고 있다- 김지훈, 할리우드 진출한다…아마존 ‘버터플라이’ 주연 합류
- “도박자금 마련하려고”…시험장 화장실서 답안 건넨 전직 토익 강사
- 몸 속에 거즈 5개월 방치…괄약근 수술 의사 입건
- 일본 여행시 섭취 주의…이 제품 먹고 26명 입원
- “1인 안 받는 이유 있었네”…식탁 위 2만원 놓고 간 손님 ‘훈훈’
 포옹·악수·뽀뽀… ‘스킨십’, 육체적·정신적 고통 줄여주는 묘약
포옹·악수·뽀뽀… ‘스킨십’, 육체적·정신적 고통 줄여주는 묘약 흑석 아파트에 ‘서반포’ 붙인다고?…집값 프리미엄 꼼수 떠들썩
흑석 아파트에 ‘서반포’ 붙인다고?…집값 프리미엄 꼼수 떠들썩 신반포 22차 3.3㎡당 공사비 1300만원 확정…‘역대 최고가’
신반포 22차 3.3㎡당 공사비 1300만원 확정…‘역대 최고가’ “XAI, 인간의 노화 멈추는 법도 알려줄 것”
“XAI, 인간의 노화 멈추는 법도 알려줄 것” 밤에 잘 못 잔다면…이런 음식 끊어야
밤에 잘 못 잔다면…이런 음식 끊어야- 정부 ‘건설현장 불법행위’ 집중단속 실시…“일부 불법 여전”
- 편의점 택배비 인상…e커머스 ‘반품교환’ 택배비도 오른다
- 최저임금 2만원 넘자 나타난 현상…‘원격 알바’ 등장
- 백일 아기 비행기 좌석 테이블에 재워…“꿀팁” vs “위험”
- 엄마 따라 밀레-보쉬 쓰던 伊서… 삼성, 가전 최고 브랜드로











![[머니 컨설팅]사적연금 받을 때 세금 유불리 따져봐야 [머니 컨설팅]사적연금 받을 때 세금 유불리 따져봐야](https://dimg.donga.com/a/102/54/90/1/wps/ECONOMY/FEED/BIZN/124603682.2.thumb.jpg)