곧 나온다더니…코로나 치료제 감감 무소식, 왜?
김성모 기자
입력 2021-03-25 17:35 수정 2021-03-25 18:32
 © 뉴스1
© 뉴스1지난해부터 국내 제약·바이오사들이 잇달아 신종 코로나바이러스 감염증(코로나19) 치료제 개발에 뛰어들었지만 개발 성공소식은 쉽게 들려오지 않고 있다. 기존 의약품을 코로나19 치료용으로 쉽게 전환할 수 있을 것으로 기대했지만 임상 통과, 효능 입증 등에 어려움을 겪고 있다. 전문가들은 변이 등 코로나19가 장기화될 가능성을 대비해 정부와 업계가 백신 못지않게 치료제 개발에도 힘을 모아야한다는 분석을 내놓는다.
25일 제약·바이오 업계에 따르면 현재 국산 코로나19 치료제는 지난달 초 ‘1호’로 승인받은 셀트리온의 바이오 신약 ‘렉키로나’ 뿐이다. 종근당, 녹십자, 대웅제약, 부광약품, 신풍제약 등은 코로나19 치료제에 도전하고 있지만 어려움을 겪고 있다. 일부 회사들은 임상 단계를 다시 거치거나, 치료제 개발 자체를 포기한 곳도 있다.
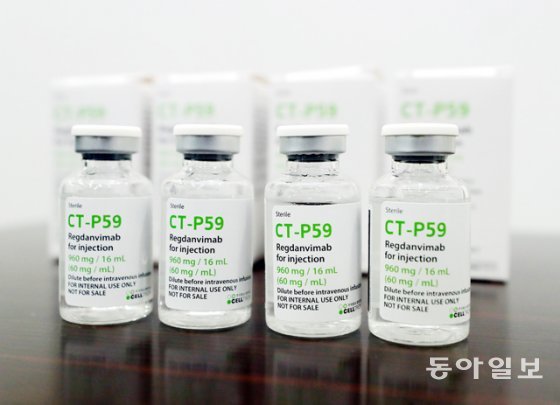 동아일보DB
동아일보DB하지만 기대에 비해 개발속도가 크게 느린 상황이다. 종근당은 췌장염 치료제 나파벨탄의 코로나19 치료제 가능성을 발견하고 임상 시험 2상을 끝내고 식약처에 조건부 승인을 요청했다. 하지만 ‘안전성·효과성 검증 자문단(검증자문단)’은 “치료 효과가 충분하지 않으며 2상 결과만으로 허가하는 것은 적절하지 않다고 판단했다”며 반려했다. 조건부 허가를 받으면 임상 3상을 진행하면서 치료제로 사용할 수 있는데 문턱을 넘지 못한 것이다.
지난달 여러 병원에서 대웅제약의 만성 췌장염 치료제 ‘호이스타정’을 코로나19 치료제로 사용하기 위해 ‘허가초과사용’을 추진했지만 불발됐다. 건강보험심사평가원이 “의학적 근거가 불충분하다”며 불승인했다. 대웅제약은 임상 시험을 거쳐 식약처로부터 허가를 받는 정식 절차를 밟고 있다. 일양약품은 백혈병 치료제(슈펙트)의 항바이러스 효과를 확인하고 코로나19 치료제로 개발을 시도했지만 3상에서 실패해 사실상 무산됐다.
일부 가능성도 보이고 있다. 녹십자는 혈장치료제(GC5131A)의 국내 임상 2상을 끝내고 다음달 조건부 허가를 신청할 계획이다. 이 치료제는 해외에서 미국 국립보건연구원과 글로벌 임상 3상도 진행 중이다. 녹십자 관계자는 “완치자의 항체를 활용하는 치료제라, 변이 등에 효율적으로 대처할 수 있다”며 “해외에서는 혈장을 구하는 게 상대적으로 용이한 만큼 ‘게임 체인저’가 될 수 있다”고 했다. 종근당도 치료제 효과를 어느 정도 입증한 만큼 ‘데이터 부족’이라는 원인을 해소해 다시 개발 가능성을 높일 계획이다.
김남중 서울대병원 감염내과 교수는 “백신 접종이 끝나더라도, 변이 바이러스가 확산되고 있고, ‘이중 변이’ 사례까지 등장하는 만큼 치료제 역시 중요하다”며 “치료제 개발에 수많은 비용이 들고 백신이 나오고 있는 만큼 제약사들도 고민이 많을 것이다. 정부가 국민적 합의를 거쳐 치료제 개발을 뒷받침할 필요가 있다”고 조언했다.
김성모 기자 mo@donga.com
비즈N 탑기사
 “도박자금 마련하려고”…시험장 화장실서 답안 건넨 전직 토익 강사
“도박자금 마련하려고”…시험장 화장실서 답안 건넨 전직 토익 강사 몸 속에 거즈 5개월 방치…괄약근 수술 의사 입건
몸 속에 거즈 5개월 방치…괄약근 수술 의사 입건 일본 여행시 섭취 주의…이 제품 먹고 26명 입원
일본 여행시 섭취 주의…이 제품 먹고 26명 입원 “1인 안 받는 이유 있었네”…식탁 위 2만원 놓고 간 손님 ‘훈훈’
“1인 안 받는 이유 있었네”…식탁 위 2만원 놓고 간 손님 ‘훈훈’ 10만원짜리 사탕?…쓰레기통까지 뒤져 찾아간 커플
10만원짜리 사탕?…쓰레기통까지 뒤져 찾아간 커플- 꿀로 위장한 고농축 대마 오일…밀수범 2명 구속 송치
- 송지아·윤후, 머리 맞대고 다정 셀카…‘아빠! 어디가?’ 꼬마들 맞아? 폭풍 성장
- 한소희 올린 ‘칼 든 강아지’ 개 주인 등판…“유기견이 슈퍼스타 됐다” 자랑
- 딱 한 장만 산 복권이 1등 당첨…20년간 월 700만원
- 기존 크림빵보다 6.6배 큰 ‘크림대빵’ 인기
 공사비 30% 뛰어… 멀어지는 ‘은퇴뒤 전원주택’ 꿈
공사비 30% 뛰어… 멀어지는 ‘은퇴뒤 전원주택’ 꿈 “팔겠다” vs “그 가격엔 안 사”… 아파트거래 ‘줄다리기’에 매물 月 3000건씩 ‘쑥’
“팔겠다” vs “그 가격엔 안 사”… 아파트거래 ‘줄다리기’에 매물 月 3000건씩 ‘쑥’ 명품 ‘에루샤’ 국내 매출 4조 돌파… 사회기부는 18억 그쳐
명품 ‘에루샤’ 국내 매출 4조 돌파… 사회기부는 18억 그쳐 “AI, 유럽 주방을 점령하다”… 삼성-LG 독주에 하이얼 도전장
“AI, 유럽 주방을 점령하다”… 삼성-LG 독주에 하이얼 도전장 “당하는 줄도 모르고 당한다”…SW 공급망 해킹 늘자 팔 걷은 정부
“당하는 줄도 모르고 당한다”…SW 공급망 해킹 늘자 팔 걷은 정부- 빚 못갚는 건설-부동산업체… 5대銀 ‘깡통대출’ 1년새 26% 급증
- IMF “韓, GDP 대비 정부 부채 작년 55.2%…5년뒤 60% 육박”
- 이건희, 19년전 ‘디자인 선언’한 밀라노… 삼성, 가전작품 전시회
- LH 작년 영업이익 98% 급감… 공공주택 사업까지 차질 우려
- 분식점부터 프렌치 호텔까지, 진화하는 팝업스토어